摘要
肌动蛋白丝在膜上的聚合为许多细胞过程产生力,如迁移、形态发生、内吞、吞噬和细胞器动力学。因此,异常的肌动蛋白细胞骨架动力学与各种疾病有关,包括癌症,以及免疫和神经系统疾病。了解肌动蛋白丝如何在细胞中产生力,肌动蛋白结合蛋白之间的相互作用如何调节力的产生,以及肌动蛋白调节机制如何响应机械负荷是许多细胞、发育和病理过程的核心。在过去的几年里,我们对控制肌动蛋白丝组装和拆卸的机制的理解有了实质性的进展。很明显,关键的肌动蛋白结合蛋白的活性并不仅仅受生化信号通路的调节,因为机械调节对这些蛋白至关重要。事实上,肌动蛋白细胞骨架的结构和动力学是由机械负荷直接调节的。在这里,我们讨论了关键的肌动蛋白调节因子的一般机制,通常相互协同,控制肌动蛋白丝的组装,拆卸和单体回收。通过使用肌动蛋白动力学的最新观点作为框架,我们讨论了肌动蛋白网络的力学和几何结构如何控制肌动蛋白结合蛋白,以及这如何转化为内吞作用和间充质细胞迁移中的力产生。
这是订阅内容的预览,可通过您的机构访问
访问选项
访问Nature和其他54种Nature组合期刊
获取自然+,我们最具价值的在线订阅
99€/ 30天
随时取消
中国客户的订阅信息
我们有一个专门的网站为我们的中国客户。请登录naturechina.com订阅本刊。
购买这篇文章
- 在Springer Link上购买
- 即时访问全文PDF
价格可能会在结账时计算当地税收




类似的内容被其他人浏览
参考文献
Gunning, P. W., Ghoshdastider, U., Whitaker, S., Popp, D.和Robinson, R. C.:组成和功能不同的肌动蛋白丝的进化。[j] .生物医学工程学报,2009-2019(2015)。
Akıl, C.等。肌动蛋白细胞骨架的神话起源。咕咕叫。当今。中国生物医学工程学报,2016,33(2):481 - 481。
肌动蛋白和肌动蛋白结合蛋白。冷泉港。教谕。生物通报8,a018226(2016)。
Oda, T., Iwasa, M., Aihara, T., masameda, Y.和Narita, A. .球形肌动蛋白向纤维肌动蛋白转变的本质。自然,457,441-445(2009)。
美利诺,F.等。低温电镜近原子分辨率显示ATP水解后f -肌动蛋白的结构转变。Nat。结构。生物学报,25,528-537(2018)。
周世忠,波拉德,邓文杰。用低温电镜分析三种不同核苷酸结合的肌动蛋白丝的聚合机理。自然科学进展。美国116,4265-4274(2019)。
波拉德,T. D.和库珀,J. a .肌动蛋白,细胞形状和运动的中心角色。科学通报,26(2009):128 - 1212。
Blanchoin, L, boujemmaa - paterski, R., Sykes, C.和Plastino, J.肌动蛋白动力学、结构和细胞运动力学。杂志。Rev. 94, 235-263(2014)。
应力纤维的内部工作-从收缩机械到焦点粘连和背。[j] .中国生物医学工程学报,2016,32(2):481 - 481。
Anderson, C. A, Kovar, D. R, Gardel, M. L. & Winkelman, J. D.细胞机械生物学中的LIM结构域蛋白。细胞骨架,78,303-311(2021)。
Mogilner, A.和Oster, G.聚合物马达:向前推,向后拉。咕咕叫。中国生物医学工程学报,2003,16(2):481 - 481。
Kaksonen, M., Sun, Y.和Drubin, D. G.。内吞内化过程中受体、接头和肌动蛋白的关联途径。单元115,475-487(2003)。
Lacy, M. M., Baddeley, D.和Berro, J.网格蛋白介导的内吞作用中肌动蛋白和膜外壳蛋白的单分子周转动力学。中国生物医学工程学报,2016,33(5):591 - 591。
赖凤平等。板足中Arp2/3复合物相互作用和肌动蛋白网络周转。Embo j . 27, 982-992(2008)。
肌动蛋白丝成核的热力学和动力学。生物物理学。[j] .农业科学,2001(2)。
芬克,J.等人。Profilin和formin构成强健肌动蛋白丝生长的起搏器系统。中国生物医学工程学报,2016,39(5):591 - 591。
薛,B.和罗宾逊,R. C.肌动蛋白单体的守护者。欧元。[j] .中国生物医学工程学报,2014,32(2):444 - 444。
Koestler, s.a.等。运动细胞板足中F-和g -肌动蛋白的浓度。科学通报,2009(1)。
Boujemaa-Paterski, R.等。网络异质性调节了基于肌动蛋白的运动转向。学报,8,655(2017)。
Malik-Garbi, M.等。稳态收缩肌动球蛋白网络中的缩放行为。物理学报,15,509-516(2019)。
罗德里格斯,A. J, Shenoy, S. M., Singer, R. H. & Condeelis, J.活细胞mRNA翻译的可视化。中国生物医学工程学报,2004,17(2):444 - 444。
Safer, D, Golla, R. & Nachmias, V. T.从人血小板中分离出一种5千道尔的肌动蛋白隔离肽。自然科学进展。美国87,2536-2540(1990)。
波拉德,T. D.和库珀,J. A.棘阿米巴profilin对肌动蛋白丝成核和伸长影响的定量分析。生物化学23,6631-6641(1984)。
Gautreau, A. M., Fregoso, F. E., Simanov, G.和Dominguez, R. .分支肌动蛋白网络的成核、稳定和分解。中国生物医学工程学报,2016,33(2):432 - 432(2022)。
马切斯基,L. M.等。Scar是一种wasp相关蛋白,通过Arp2/3复合物激活肌动蛋白丝的成核。自然科学进展。美国,96,3739-3744(1999)。
毕林,P.等。wasp家族蛋白的WH2和富含脯氨酸的结构域共同促进肌动蛋白丝的伸长。生物医学工程学报,37,102-121(2018)。这篇文章描述了WASP家族蛋白的聚脯氨酸序列是如何通过将具有装配能力的profile - actin复合物带到丝的倒钩末端,以及将actin单体转移到npf附近的WH2结构域来支持丝的伸长的。此外,未被占用的WH2结构域有效地将肌动蛋白网络连接到膜上。
Padrick, S. B, Doolittle, L. K, Brautigam, C. A, King, D. S.和Rosen, M. K. Arp2/3复合体由两个WASP蛋白结合并激活。自然科学进展。美国108,e472-e479(2011)。
Ti,研究所。[2],张丽娟,张丽娟,张丽娟,等。Arp2/3络合物上促核因子WASp-VCA结合位点的结构和生化特性。自然科学进展。USA 108, e463-e471(2011)。
Zimmet, A.等。npf结合人Arp2/3复合物的低温电镜结构及活化机制。科学。机械工程学报,2016,(6):1145 - 1145。
Shaaban, M, Chowdhury, S. & Nolen, B. J. Cryo-EM揭示了Arp2/3复合物从无活性到能核态的转变。Nat。结构。中国生物医学工程学报,2016,32(2):444 - 444(2020)。
Blanchoin, L.等。直接观察由Arp2/3复合物和WASP/Scar蛋白构成核的树突状肌动蛋白丝网络。《自然》第4卷,第7 - 11期(2000)。
史密斯,b.a.等人。三色单分子成像显示WASP脱离Arp2/3复合体触发肌动蛋白丝分支的形成。中国生物医学工程学报,2013,31(2):481 - 481。
杨建军,杨建军,杨建军,等。Arp2/3复合物和肌动蛋白解聚因子/cofilin在板状足树突组织中的作用。中国生物医学工程学报,2009,32(2):481 - 481。
Mullins, R. D, Heuser, J. A. & Pollard, T. D. Arp2/3复合物与肌动蛋白的相互作用:成核、高亲和力的尖端盖帽和细丝分支网络的形成。自然科学进展。美国95,6181-6186(1998)。
Kovar, D. R. & Pollard, T. D.肌动蛋白丝的插入组装与形成蛋白相关的刺端产生皮牛顿力。自然科学进展。美国101,14725-14730(2004)。
罗梅罗,S.等。双胍是一种进程马达,需要profilin来加速肌动蛋白的组装和相关的ATP水解。Cell 119, 419-429(2004)。
形成蛋白介导的肌动蛋白组装和动力学机制。生物物理学。Rev. 10, 1553-1569(2018)。
Watanabe, N., Kato, T., Fujita, A., Ishizaki, T.和Narumiya, S. mDia1和ROCK在rho诱导的肌动蛋白重组中的合作。新细胞生物学,1,136 - 143(1999)。
Ramalingam, N.等。磷脂调节甲双胍的定位和活性。欧元。中国生物医学工程学报,2009,33(2):444 - 444。
Gorelik, R., Yang, C., Kameswaran, V., Dominguez, R.和Svitkina, T.通过其氨基末端结构域的质膜靶向formin mDia2的机制。摩尔。杂志。Cell 22, 189-201(2011)。
Pring, M., Evangelista, M., Boone, C., Yang, C.和Zigmond, S. H.肌动蛋白丝形成蛋白诱导成核的机制。生物化学42,486-496(2003)。
贝克,j.l.等。Bni1p formin FH2结构域与肌动蛋白之间的静电相互作用影响肌动蛋白丝的成核。结构23,68-79(2015)。
古尔德,c.j.等。formin DAD结构域在自抑制和肌动蛋白成核中起双重作用。咕咕叫。生物学报,21,384-390(2011)。
Thompson, M. E, Heimsath, E. G, Gauvin, T. J, Higgs, H. N.和Kull, F. J. FMNL3 fh2 -肌动蛋白结构揭示了formin介导的肌动蛋白成核和延伸。Nat。结构。生物化学学报,2000,26(3):444 - 444(2013)。
莫斯利,j.b.等。Bni1-和mdia1诱导肌动蛋白组装的保守机制以及Bud6和profilin对Bni1的双重调控。摩尔。杂志。Cell 15, 896-907(2004)。
谢旸,等。极化体支架spa2介导Aip5大分子缩聚用于肌动蛋白聚合。Nat. common . 10,5078(2019)。
Okada, K.等人。大肠腺瘤性息肉病蛋白形成肌动蛋白组装并与甲酰基蛋白协同作用。中国生物医学工程学报,2009,32(2):481 - 481。
昆兰,m.e.,希尔格特,S., Bedrossian, A.,穆林斯,R. D.和Kerkhoff, E.两个肌动蛋白成核器,Spire和卡布奇诺之间的调节相互作用。中国生物医学工程学报,2009,32(2):481 - 481。
na/VASP蛋白在细胞边缘突出、迁移和粘附中的作用。[j] .中国生物医学工程学报,2016,32(2):481 - 481。
Disanza, A.等。CDC42通过VASP的聚集将IRSp53从抑制肌动蛋白生长转变为延长。中国生物医学工程学报,2013,31(2):444 - 444。
Breitsprecher等人。Ena/ vasp介导的肌动蛋白丝伸长的分子机制。Embo j . 30, 456-467(2011)。
Ferron, F., Rebowski, G., Lee, S. H.和Dominguez, R. . Ena/VASP在纤维伸长过程中聚集的结构基础。中国生物医学工程学报,26,(2007)。
贝尔,j.e.等人。Ena/VASP蛋白与肌动蛋白丝盖的拮抗作用调节成纤维细胞的运动。单元109,509-521(2002)。
VASP是一种进行性肌动蛋白聚合酶,需要单体肌动蛋白进行倒钩端结合。中国生物医学工程学报,2009,32(2):444 - 444。
Winkelman, J. D., Bilancia, C. G., Peifer, M. & Kovar, D. R. Ena/VASP Enabled是一种高度程序化的肌动蛋白聚合酶,可与束状蛋白自组装平行捆绑的f-肌动蛋白网络。自然科学进展。USA 111, 4121-4126(2014)。
Breitsprecher等人。VASP的聚集性积极地推动了WH2结构域介导的肌动蛋白丝的延长。中国生物医学工程学报,2009,33(2):444 - 444。
Barzik, M.等。在有倒钩端盖蛋白存在的情况下,Ena/VASP蛋白增强肌动蛋白聚合。生物。化学,2853 - 28662(2005)。
凯奇,F.等。FMNL成形促进板足力的产生。学报,8,14832(2017)。这项研究表明,除了Arp2/3复合物外,由formins催化的肌动蛋白聚合对于板状肌动蛋白丝网络的正常结构和功能也很重要。
Damiano-Guercio等人。Ena/VASP的缺失会干扰板基结构、运动性和整合素依赖性粘附。中国生物医学工程学报,2016,33(2):481 - 481。
Svitkina, t.m.等人。树突网络重组产生丝状伪足的机制。中国生物医学工程学报,2003,16(2):444 - 444。
约翰逊,h.e.等。f -肌动蛋白束通过黏附信号传导指导板足的起始和方向。[j] .中国生物医学工程学报,2015,33(2):444 - 444。
阿查德,V.等。基于“引物”的机制是分支肌动蛋白丝网络形成和运动的基础。咕咕叫。生物学报,20,423-428(2010)。
Raz-Ben arousal, D.等。板足碎片中的肌动蛋白周转。咕咕叫。生物学杂志27,2963-2973。e14灯头(2017)。
Smith, m.b, Kiuchi, T., Watanabe, N.和Vavylonis, D.板状基板中的分布肌动蛋白周转和FRAP动力学。生物物理学。[j] .农业科学,2013,(4)。
Vitriol, E. A.等。两种功能不同的肌动蛋白单体来源供应板足的前缘。Cell rep 11, 433-445(2015)。
cofilin切断肌动蛋白丝,使肌动蛋白贴片解体,并产生新的贴片的母丝。咕咕叫。中国生物医学工程学报,2013,33(2):444 - 444。
Wioland, H.等。ADF/Cofilin通过切断细丝并促进其两端的解聚来加速肌动蛋白动力学。咕咕叫。生物学27,1956-1967。e7(2017)。这篇文章揭示了ADF/cofilin饱和的丝的刺端很难盖住,即使在肌动蛋白单体存在的情况下,它们也会解聚。对三种哺乳动物同种异构体,所有支撑丝切断和两端解聚的反应都进行了量化。
Blanchoin, L, Pollard, T. D. & Mullins, R. D. ADF/cofilin, Arp2/3复合物,capping蛋白和profilin在分支肌动蛋白丝网络重塑中的相互作用。咕咕叫。中国生物医学工程学报,2009,32(2):481 - 481。
Cofilin从肌动蛋白丝中分离Arp2/3复合体和分支。咕咕叫。生物学报,19,537-545(2009)。
施罗德,t.a.。为基础。中国生物医学工程学报,2004,32(2):759-779。
Urnavicius, L.等。动力蛋白复合物的结构及其与动力蛋白的相互作用。科学通报,36(5):441 - 446(2015)。
福金,a.i.等。动力蛋白的Arp1/11微丝启动内体Arp2/3复合体。科学。ad7, eabd5956(2021)。这篇文章表明,在核内体的表面,WASH复合体与动肌蛋白相互作用,解开Arp1/11微丝,启动依赖于WASH的核内体Arp2/3分支肌动蛋白网络。
Wagner, A. R., Luan, Q., Liu, s - l .。Dip1定义了一类Arp2/3复合体激活剂,其功能不需要预先形成的肌动蛋白丝。咕咕叫。生物学报,23,1990-1998(2013)。
Cao, L.等。SPIN90与mDia1和Arp2/3复合物结合,调节皮质肌动蛋白的组织。生物医学工程学报,2016,33(2):481 - 481(2020)。本文研究了SPIN90如何在细胞中促进Dia1生成的皮层,并揭示了SPIN90 - arp2 /3 - Dia1复合体的形成,该复合体在体外增强了丝的成核,使丝快速伸长,Dia1位于刺端,SPIN90 - arp2 /3位于尖端。
Balzer, C. J, Wagner, A. R, Helgeson, L. A.和Nolen, B. J. Dip1对Arp2/3复合体的单次激活可能会平衡线状和支状肌动蛋白丝的成核。咕咕叫。生物学报,29,3331-3338。e7(2019)。
巴尔泽,C. J.等。Wsp1和Dip1之间的协同作用可能启动内吞肌动蛋白网络的组装。中国生物医学工程学报,2016,33(6):444 - 444。
Lamellipodin通过聚集Ena/VASP蛋白并将其拴在肌动蛋白丝上来促进肌动蛋白的组装。中国生物医学工程学报,2015,39(5):481 - 481。
Dimchev, G.等。板足素通过稳定突起和促进粘连形成来调节细胞迁移。[j] .细胞科学,2012,32(2):481 - 481。
Cheng, K. W.和Mullins, R. D.含有VASP和板足素的丝状足尖端复合物的启动和分解。摩尔。杂志。31 Cell, 2021-2034(2020)。
Zigmond, s.h.等人。双胍漏帽允许在紧盖蛋白的存在下延长。咕咕叫。《生物学》13,1820-1823(2003)。
Shekhar, S.等。双胍蛋白和封盖蛋白一起包裹在肌动蛋白丝上,形成一个网状结构。学报,6,8730(2015)。
庞巴迪,j.p.等。肌动蛋白丝倒钩端形成蛋白封盖蛋白“决定复合体”的单分子可视化。Nat. common . 6,8707(2015)。
哈克,a.j.等。Ena/VASP的进程伸长是由丝足交联剂束蛋白捆绑的肌动蛋白丝的亲和度调节的。摩尔。杂志。Cell 30, 851-862(2019)。
芬克,J.等人。一个倒钩端干扰机制揭示了帽蛋白如何促进分支肌动蛋白网络的成核。联邦法典,12,5329(2021)。这篇文章解释了CP通过阻止Arp2/3 NPF与丝的刺端结合,从而增强了Arp2/3复合物通过肌动蛋白丝的成核,从而有利于NPF加载激活Arp2/3复合物进行分支网络组装所需的肌动蛋白单体。
威斯纳,S.等。仿生运动分析提供了深入了解基于肌动蛋白的运动机制。中国生物医学工程学报,2003,19(3):387-398(2003)。
Loisel, t.p, Boujemaa, R., Pantaloni, D.和Carlier, m.f。用纯蛋白重建李斯特菌和志贺氏菌的肌动蛋白运动。《自然》(英文版),1999年第1期。
波拉德,T. D., Blanchoin, L.和Mullins, R. D.控制肌动蛋白丝动力学的分子机制。为基础。启Biophys。Biomol。结构。29,545-576(2000)。
Bamburg, J. R, Harris, H. E.和weed, A. G.脑肌动蛋白解聚因子的部分纯化和表征。快报121,178-182(1980)。
Cofilin促进体内肌动蛋白丝的快速更新。《自然》388,78-82(1997)。
Andrianantoandro, E. & Pollard, T. D.不同浓度ADF/cofilin下肌动蛋白丝的断裂和成核机制。Mol. Cell 24, 13-23(2006)。
McGough, A., Pope, B., Chiu, W.和weed, A. Cofilin改变f-actin的扭曲:对actin丝动力学和细胞功能的影响。中国生物医学工程学报,2003,14(2):481 - 481。
苏亚雷斯,C.等。Cofilin调节肌动蛋白丝的核苷酸状态,并在裸段和装饰段边界切断。咕咕叫。生物学报,21,862-868(2011)。
田中,K.等。cofilin结合和actin丝分解的结构基础。Nat. common . 9, 1860(2018)。
Huehn, a.r.等。cofilin诱导的结构变化揭示了肌动蛋白丝的局部和不对称扰动。自然科学进展。美国117,1478-1484(2020)。
卡莉,M.-F。et al。肌动蛋白解聚因子(ADF/cofilin)提高丝的周转速度:与肌动蛋白为基础的运动有关。中国生物医学工程学报,2003,19(4):444 - 444。
Shekhar, S.和Carlier, M.-F.;ADF/cofilin促进肌动蛋白丝的解聚和封顶蛋白的单体聚集共同加速了刺端生长。咕咕叫。生物学27,1990-1998。e5(2017)。
Wioland, H., Jegou, A.和Romet-Lemonne, G.肌动蛋白解聚因子/Cofilin对肌动蛋白丝的多重作用随pH的定量变化。生物化学58,40-47(2019)。
Balcer, h.i.等。高分子量Srv2/CAP复合物、cofilin、profilin和Aip1协同调节肌动蛋白丝的周转。咕咕叫。中国生物医学工程学报,2003,22(3):559 - 569。
环化酶相关蛋白在果蝇和酵母的卵发生过程中调控肌动蛋白和细胞极性。咕咕叫。生物工程学报,2009,32(2):444 - 444。
伯特林,E.等。环化酶相关蛋白1 (CAP1)促进哺乳动物非肌肉细胞中cofilin诱导的肌动蛋白动力学。摩尔。杂志。15单元,2324-2334(2004)。
Moriyama, K. & Yahara, I.人类CAP1是cofilin和actin快速周转循环的关键因素。[j] .中国生物医学工程学报,2003,19(4):444 - 444。
Gressin, L, Guillotin, A, guassarin, C, Blanchoin, L. & Michelot, A.肌动蛋白丝网络分解的结构依赖。咕咕叫。生物学报,25,1437-1447(2015)。
Kotila, T.等。环化酶相关蛋白与辅纤蛋白协同肌动蛋白丝尖端解聚的机理。Nat. common . 10,5320(2019)。本研究证实了CAP催化cofilin-actin丝的尖端解聚,并揭示了其潜在的结构机制。
Shekhar, S., Chung, J., Kondev, J., Gelles, J. & Goode, B. L.环化酶相关蛋白和cofilin的协同作用加速肌动蛋白丝解聚的两个数量级。Nat. common . 10,5319(2019)。研究表明,CAP可加速肌动蛋白丝尖端解聚。
Kotila, T.等。环化酶相关蛋白对肌动蛋白单体再充电的结构基础。Nat. common . 9,1892(2018)。
Freeman, N. L., Chen, Z., Horenstein, J., Weber, A.和Field, J.一个肌动蛋白单体结合活性定位于酿酒酵母环化酶相关蛋白的羧基末端。生物。化学,270,5680 - 5685(1995)。
Brieher, W. M., Kueh, H. Y., Ballif, B. A.和Mitchison, T. J.用cofilin, coronin和Aip1快速解聚李斯特菌肌动蛋白彗尾。中国生物医学工程学报,2004,26(2):444 - 444。
Kueh, H. Y., Charras, G. T., Mitchison, T. J. & Brieher, W. M.肌动蛋白被cofilin, coronin和Aip1分解发生在爆发中,并被带刺末端帽子抑制。中国生物医学工程学报,2009,33(2):444 - 444。
詹森,S.等。三组分有序肌动蛋白分解机制的单分子成像。学报,6,7202(2015)。
Chen, Q., Courtemanche, N. & Pollard, T. D. Aip1通过cofilin促进肌动蛋白丝的切断,并调节细胞动力学收缩环的收缩。生物。化学,299,2289 - 2300(2015)。
Rodal, A. A., Tetreault, J. W., Lappalainen, P., Drubin, D. G.和Amberg, D. C. Aip1p与cofilin相互作用,分解肌动蛋白丝。中国生物医学工程学报,2009,32(2):481 - 481。
Aip1通过切断和加速单体从末端解离来破坏饱和cofilin的肌动蛋白丝的稳定性。咕咕叫。中国生物医学工程学报,2014,27(4):559 - 567。
肌动蛋白相互作用蛋白1 (AIP1)/WD重复蛋白1 (WDR1)在肌动蛋白丝动力学和细胞骨架调控中的功能。物化学。生物物理学。《共同法典》第506期,315-322(2018)。
Okada, K.等人。爪蟾肌动蛋白相互作用蛋白1 (Xenopus actin-interacting protein 1, XAip1)通过封盖丝端来促进丝的cofilin断裂。生物。化学,277,43011-43016(2002)。
唐文伟,Nadkarni, A. V. & Brieher, W. M. cofilin, Aip1和coronin导致的肌动蛋白丝断裂。生物。化学通报,2016,36(2):444 - 444。
Cai, L, Makhov, A. M. & Bear, J. E. f -肌动蛋白结合对体内冠状蛋白1B的功能至关重要。[j] .中国生物医学工程学报,2003,17(4):481 - 481。
Ge, P, Durer, Z. A. O, Kudryashov, D, Zhou, Z. h和Reisler, E. Cryo-EM揭示了ADP -和ADP - befx肌动蛋白丝的不同冠蛋白结合模式。Nat。结构。生物学报,21,1075-1081(2014)。
汉弗莱斯,c.l.等。肌动蛋白结合蛋白冠蛋白对Arp2/3复合物活性和功能的直接调控。中国生物医学工程学报,2003,19(2):444 - 444。
Cai, L, Marshall, T. W., Uetrecht, A. C, Schafer, D. A.和Bear, J. E. Coronin 1B在前沿协调Arp2/3复合物和cofilin活动。Cell 128, 915-929(2007)。
Cai, L., Makhov, A. M., Schafer, D. A.和Bear, J. E.。在板足中,Coronin 1B拮抗接触蛋白并重塑含有arp2 /3的肌动蛋白分支。Cell 134, 828-842(2008)。
Rodal, a.a.等人。Arp2/3复合物构象变化导致肌动蛋白成核。Nat。结构。摩尔生物学,12,26-31(2005)。
刘,S.-L。,李建平,李建平,李建平,李建平,李建平,李建平。冠状蛋白对Arp2/3复合体激活和抑制的作用机制。生物。化学,286,17039-17046(2011)。
阿贝拉,j.v.g.等。Arp2/3复合体的异构体多样性决定了肌动蛋白丝的动力学。细胞生物学,18,76-86(2016)。
Luan, Q. & Nolen, B. J. GMF调控Arp2/3复合物的结构基础。Nat。结构。生物工程学报,2016,32(2):444 - 444(2013)。
甘地等人。GMF是一种cofilin同源物,结合Arp2/3复合物刺激纤维脱支并抑制肌动蛋白成核。咕咕叫。中国生物医学工程学报,2016,32(2):481 - 481(2010)。
Boczkowska, M., Rebowski, G.和Dominguez, R. .神经胶质成熟因子(GMF)以核苷酸状态依赖的方式与Arp2/3复合物相互作用。生物。化学通报,2013,33(4):481 - 481。
Schafer, D. A, Jennings, P. B. & Cooper, J. A.体外封盖蛋白和肌动蛋白组装的动力学:通过多磷酸肌苷解开带刺末端的封盖。中国生物医学工程学报,35(5),349 - 349(1996)。
Miyoshi, t。树突成核肌动蛋白网络中封盖蛋白的快速解离:频繁的丝切断的证据。中国生物医学工程学报,2003,19(2):444 - 444(2006)。
哈卡拉,M.等。双丝蛋白打开丝的倒钩末端,促进板足肌动蛋白网络的周转。中国生物医学工程学报,2014,33(2):444 - 444。本研究表明,在体外和细胞中,twinfilin可使肌动蛋白丝脱帽,并促进肌动蛋白丝倒钩端解聚。
Shekhar, S, Hoeprich, G. J, Gelles, J. & Goode, B. L. Twinfilin绕过装配条件和肌动蛋白丝老化驱动倒钩端解聚。[j] .生物医学工程学报,2016,33(2):481 - 481。
李建军,李建军,李建军,等。一种广泛存在的肌动蛋白单体分离蛋白-双联蛋白对出芽酵母皮层肌动蛋白细胞骨架的调控。中国生物医学工程学报,32(2),344 - 344(1998)。
Mwangangi, D. M., Manser, E.和Robinson, R. C. .肌动蛋白丝脱帽复合体的结构。科学。生物医学工程学报,2017,30(2)。
Helfer, E.等。哺乳动物双联蛋白隔离adp - g -肌动蛋白并盖住丝倒钩末端:运动的意义。中华医学杂志,25,(2006):1184-1195。
福尔克,S.等。双环蛋白-封盖蛋白相互作用的生物学作用和结构机制。中国生物医学工程学报,2009,32(2):444 - 444。
约翰斯顿,a.b.等人。一种由双螺旋蛋白调控的新模式。中国生物医学工程学报,2018,33(4):481 - 481。
荣格等人。V-1在体内调节capping蛋白活性。自然科学进展。美国113,e6610-e6619(2016)。
Shekhar, S., Pernier, J.和Carlier, m - f .。肌动蛋白调控丝的倒钩末端一目了然。[j] .中国生物医学工程学报,2016,32(2):481 - 481。
阴离子磷脂对鸡肌肉肌动蛋白封盖蛋白CapZ的调控作用。生物化学30,8753-8758(1991)。
Stark, B. C, Lanier, M. H. & Cooper, J. A. CARMIL家族蛋白在肌动蛋白运动中的多域调控作用。摩尔。杂志。单元28,1713-1723(2017)。
在运动细胞中,应力纤维由两种不同的肌动蛋白组装机制产生。中国生物医学工程学报,2003,19(3):387 - 394(2006)。
Fritzsche, M., Erlenkämper, C., Moeendarbary, E., Charras, G.和Kruse, K.肌动蛋白动力学塑造皮层网络结构和力学。科学。ad2, e1501337(2016)。
Lawson, c.d.和Ridley, A. J. Rho GTPase信号复合物在细胞迁移和侵袭中的作用。[j] .中国生物医学工程学报,2016,33(2):457 - 457(2018)。
Senju, Y.和Lappalainen, P. PI(4,5)P2调控肌动蛋白动力学在细胞迁移和内吞作用中的作用。咕咕叫。当今。中国生物医学工程学报,2016,33(4):444 - 444。
Mehidi, A.等。板足肌动蛋白丝伸长产生的力在细胞迁移过程中调节WAVE复合体。中国生物医学工程学报,2016,33(2):444 - 444。本文描述了在板足中,源自单个肌动蛋白丝伸长的力如何局部控制WRC的捕获和激活及其下游原位Arp2/3复合物的激活。波的横向运动平行于板基顶端,突出了该区域纤维取向的复杂性。
毕林,P.等。力反馈控制自组装分支肌动蛋白网络的运动活动和机械性能。Cell 164, 115-127(2016)。
李,T.-D。, Bieling, P., Weichsel, J., Mullins, R. D.和Fletcher, D. A.:支链肌动蛋白网络负荷适应的分子机制。预印本在bioRxiv https://doi.org/10.1101/2021.05.24.445507(2021)。本研究揭示了布朗棘轮控制着分支肌动蛋白网络稳态生长的负荷适应。纤维伸长和Arp2/3纤维分支的减少伴随着纤维倒钩末端旋盖的减少,导致分支网络更加密集。
奥克斯,p.w.等。光遗传调控RhoA揭示了酵素介导的应力纤维弹性。学报,8,15817(2017)。
Winkelman, J. D., Anderson, C. A., Suarez, C., Kovar, D. R.和Gardel, M. L.进化上不同的LIM结构域蛋白通过保守机制结合应激肌动蛋白丝。自然科学进展。美国117,25532-25542(2020)。
Sun, X.等。通过LIM结构域直接结合张力f -肌动蛋白的机械传感。55号牢房,468-482。e7(2020)。
Risca, V. I.等。肌动蛋白丝曲率偏向分支方向。自然科学进展。《美国科学》(英文版),2012(5)。
Dogterom, M.和Yurke, B.生长微管的力-速度关系的测量。《科学》第28卷,第856 - 856页(1997)。
jsamu, A., Carlier, M.-F。Formin mDia1感知并在肌动蛋白丝上产生机械力。Nat. common . 4, 1883(2013)。
李俊英,波拉德,T. D.和格林,E. C.张力调节肌动蛋白丝聚合的双胍和profilin介导。自然科学进展。美国110,9752-9757(2013)。
Kubota, H.等。profilin的双相效应影响肌动蛋白聚合中formin mDia1的力感机制。生物物理学。[j] .科学通报,2012,(1)。
在f -肌动蛋白丝聚合过程中,mDia1同时感知力和扭矩。合议。8,1650(2017)。
齐默尔曼等人。机械调节抑制双胍促进收缩肌动球蛋白环组装。学报,8,703(2017)。
瓦伦西亚,f.r.等。肌动蛋白延伸因子mDia1的力依赖性激活保护细胞骨架免受机械损伤并促进应力纤维修复。56号室,3288-3302。e5(2021)。
Cao, L.等。轮廓和机械张力对双胍加工能力的调节。中国生物医学工程学报,2018,34(6)。
铃木,e.l.等人。几何约束极大地阻碍了mDia1活动的形成。生物工程学报,2016,32(2020)。
机械调节肌动蛋白丝以调节肌动蛋白结合蛋白的作用。咕咕叫。当今。中国生物医学工程学报,2016,32(2):444 - 444。
Pimpale, L. G., Middelkoop, T. C., Mietke, A. & Grill, S. W.细胞谱系依赖性手性肌动球蛋白流动驱动秀丽隐杆线虫早期发育的细胞重排。中国生物医学工程学报,2016,33(6):591 - 591。
Tee, Y. H.等。由肌动蛋白细胞骨架的自组织引起的细胞手性。中国生物医学工程学报,2016,33(5):555 - 557(2015)。
Lebreton, G.等。保守的肌球蛋白1D诱导分子到有机体的手性。科学学报,362,949-952(2018)。
Kishino, a .和Yanagida, T.用玻璃针对单个肌动蛋白丝进行微操作的力测量。《自然》334,74-76(1988)。
Tsuda, Y., Yasutake, H., Ishijima, A. & Yanagida, T.,通过体外显微操作直接测量单个肌动蛋白丝的扭转刚度和肌动蛋白-肌动蛋白键断裂力。自然科学进展。美国93,12937-12942(1996)。
潘迪特,n.g.等。Arp2/3复合物的力和磷酸盐释放促进肌动蛋白丝分支的解离。自然科学进展。(美国)117,13519-13528(2020)。本文表明,当对子丝施加2-pN拉力而不对母丝施加2-pN拉力时,裂变酵母Arp2/3分支结的脱支速度加快了两个数量级。“老”ADP-Arp2/3复合物对拉力和裂变酵母GMF的脱支敏感性是“年轻”ADP-Pi复合物的20倍。
Pernier, J.等。Myosin 1b使肌动蛋白分支变平并修剪。[j] .生物医学工程学报,2016,42(1)。
Vignaud, T.等。应力纤维嵌入在可收缩的皮质网络中。自然科学学报,20,410 - 420(2021)。
梅,L.等。α-连环蛋白直接感应肌动蛋白力的分子机制。中国生物工程学报,2016,32(6):626 - 626(2020)。
Hayakawa, K, Tatsumi, H. & Sokabe, M.肌动蛋白丝的张力依赖性结合作为张力传感器的功能。中国生物医学工程学报,2014,32(2):444 - 444。
Wioland, H., Jegou, A.和Romet-Lemonne, G.交联肌动蛋白丝上ADF/cofilin产生的扭转应力促进了它们的断裂。自然科学进展。美国116,2595-2602(2019)。这篇文章表明,扭转约束的细丝经历了一个机械扭矩在粘丝结合,大大提高了他们的切断。此外,丝的曲率有利于剪断,但张力几乎没有任何影响。
Pavlov, D., Muhlrad, A., Cooper, J., Wear, M.和Reisler, E.用cofilin切断肌动蛋白丝。中国生物医学工程学报,2003,19(3):559 - 558(2007)。
吴,C.等。Arp2/3对板足和对细胞外基质信号的反应至关重要,但对趋化性是必不可少的。Cell 148, 973-987(2012)。
Krause, M. & Gautreau, A.引导细胞迁移:板状基底动力学和定向持久性的调节。中华生物医学工程学报,2015,33(5):577-590。
凯斯,l.b.和沃特曼,c.m.肌动蛋白动力学和细胞粘附的三维机械敏感分子离合器集成。中国生物医学工程学报,2016,33(5):559 - 563(2015)。
Vitriol, E. A., Wise, A. L., Berginski, M. E., Bamburg, J. R.和Zheng, J. Q.。cofilin的瞬时失活揭示了F-actin在板足中的分解功能。摩尔。杂志。Cell 24, 2238-2247(2013)。
罗蒂,j.d.等人。Profilin-1通过arp2 /3依赖性和非依赖性途径作为肌动蛋白组装的看门人。开发单元32,54-67(2015)。
Poukkula等人。转基因生物促进前沿动态和集体细胞迁移在体内。咕咕叫。中国生物医学工程学报,2014,33(2):444 - 444。
Chaudhuri, O, Parekh, S. H. & Fletcher, D. A.肌动蛋白网络可逆应力软化。自然,445,295-298(2007)。
Bauër, P.等。一种测量分支肌动蛋白网络力学和动态装配的新方法。科学。众议员7,15688(2017)。
穆勒,J.等。板足肌动蛋白网络的负载自适应。171号,188-200号牢房。e16天(2017)。这篇文章证明了细胞中片状肌动蛋白丝网络的密度和结构适应负载。
加纳,R. M. & Theriot, J. A.迁移细胞的前沿维持是分支肌动蛋白网络生长的一个紧急特性。中国生物医学工程学报,2016,33(2):481 - 481。
吕荣,朱斌,邓国光,孙玉玉。芽孢酵母中网格蛋白介导的内吞作用。[j] .中国生物医学工程学报,2016,32(2):481 - 481。
Kaksonen, M. & Roux, A.网格蛋白介导的内吞作用机制。中国生物医学工程学报,2016,33(2):313-326(2018)。
酵母和哺乳动物内吞作用对肌动蛋白的不同需求。中国生物医学工程学报,2009,32(2):444 - 444。
Boulant, S., Kural, C., Zeeh, j.c。, Ubelmann, F. & Kirchhausen, T.肌动蛋白动力学抵消网格蛋白介导的内吞作用中的膜张力。中华生物医学工程学报,2011,31(4):559 - 561。
蒙德,M.等。系统的纳米级内吞作用分析将有效的囊泡形成与肌动蛋白成核联系起来。174号牢房,884-896。e17(2018)。
Almeida-Souza, L.等。扁平的BAR蛋白促进肌动蛋白在网格蛋白包覆的凹坑底部聚合。174室,325-337室。e14灯头(2018)。
Akamatsu, M.等。在网格蛋白介导的内吞过程中,肌动蛋白细胞骨架的自组织和负荷适应原理。中国生物医学工程学报,2016,33(6):1145 - 1145。本文表明,内吞肌动蛋白丝网络对负载有响应。作者还揭示了这些结构中的肌动蛋白丝弯曲以储存弹性能量。
Serwas, D.等。囊泡形成中肌动蛋白力的产生:来自低温电子断层扫描的机制见解。预印本在bioRxiv https://doi.org/10.1101/2021.06.28.450262(2021)。
Skruzny等人。在网格蛋白介导的内吞过程中,质膜与肌动蛋白细胞骨架耦合的分子基础。自然科学进展。美国学报(英文版)109,e2533-e2542(2012)。
Abella, M., Andruck, L., Malengo, G.和Skruzny, M.用基于sla2的FRET张力传感器测量肌动蛋白在胞吞过程中产生的力。56号房,2419-2426。e4(2021)。
Manenschijn, h.e.等。i型肌球蛋白促进肌动蛋白聚合,在胞吞过程中驱动膜弯曲。中国生物医学工程学报,2016,33(4):444 - 444。
在网格蛋白介导的胞吞过程中,I型肌凝蛋白锚定肌动蛋白组装到质膜上。[j] .中国生物医学工程学报,2016,33(2):481 - 481(2019)。
Sirotkin, V., Berro, J., Macmillan, K., Zhao, L.和Pollard, T. D.裂变酵母内噬肌动蛋白贴片组装和拆卸机制的定量分析。摩尔。杂志。Cell 21, 2894-2904(2010)。
Taylor, M. J, Perrais, D.和Merrifield, C. J.对哺乳动物网格蛋白介导的内吞作用分子动力学的高精度调查。生物科学进展,2016,33(4):481 - 481。
Kaksonen, M., Toret, C. P.和Drubin, D. G.:网格蛋白和肌动蛋白介导的内吞机制的模块化设计。Cell 123, 305-320(2005)。
Toshima, J. Y.等。在网格蛋白介导的内吞过程中,Srv2/CAP是极化肌动蛋白电缆组装和贴片内化所必需的。[j] .中国生物医学工程学报,2016,32(2):481 - 481。
m .肌动蛋白聚合力的放大。[j] .中国生物医学工程学报,2016,33(2):444 - 444。
卡普兰等人。内吞肌动蛋白网络的负荷适应。摩尔。杂志。细胞https://doi.org/10.1091/mbc.E21-11-0589(2022)。
blancchoin, L.和Pollard, T. D.棘阿米巴actophorin (ADF/cofilin)与肌动蛋白丝相互作用机制。生物。化学,274,15538-15546(1999)。
苏亚雷斯,C.等。Profilin调节F-actin网络的稳态,其机制是formin优于Arp2/3复合物。开发单元32,43-53(2015)。
斯克鲁伯等人。Arp2/3和Mena/VASP需要profilin1在前沿进行肌动蛋白网络组装。咕咕叫。生物学报,30,2651-2664。e5(2020)。
Mohapatra, L., Lagny, T. J., Harbage, D., Jelenkovic, P. R.和Kondev, J.限制池机制不能控制多个细胞器的大小。细胞系统,4,559 - 567。e14灯头(2017)。
在普通细胞质中构建不同的肌动蛋白丝网络。咕咕叫。生物学报,21,560-569(2011)。
Antkowiak, A.等。共享一个共同环境的肌动蛋白网络的大小是由组装的相对速率决定的。中国生物医学工程学报,2016,33(4):481 - 481。
Burnette, d.t.等人。肌动蛋白在迁移细胞的前沿推进中的作用。中国生物医学工程学报,2011,31(4):371-382。
Lehtimäki, j.i, Rajakylä, e.k, Tojkander, S. & Lappalainen, P.肌动蛋白皮层重组中应力纤维的产生。中国生物工程学报,2016,32(2):481 - 481。
A. reverat等人。利用环境地形的细胞运动。《自然》(英文版),2016年第5期。
盖特纳,F.等。WASp触发机械敏感肌动蛋白贴片,促进免疫细胞在致密组织中的迁移。57室,47-62室。e9(2022)。
Simunovic, M., Evergren, E., Callan-Jones, A.和Bassereau, P.细胞内外弯曲:BAR结构域蛋白在膜形成中的作用及其细胞意义。为基础。[j] .中国生物医学工程学报,2016,31(2):481 - 481。
由肌动蛋白丝的组装和拆卸驱动的细胞运动。Cell 112, 453-465(2003)。
jsamou, A.等。微流体中的单个肌动蛋白细丝揭示了ATP水解的机制,并深入了解了profilin的特性。生物科学进展,2011,31(2):481 - 481。
罗森布鲁姆,A. D.,科瓦尔,E. W.,科瓦尔,D. R.,勒夫,L. M.和波拉德,T. D.肌动蛋白丝成核的机制。生物物理学。[j] .科学通报,2012(1):1 - 4。
作者信息
作者及单位
贡献
作者对文章的各个方面都作出了平等的贡献。
相应的作者
道德声明
相互竞争的利益
作者声明没有竞争利益。
同行评审
同行评议信息
自然评论分子细胞生物学感谢Klemens Rottner, David Kovar,他们与Cristian Suarez以及其他匿名审稿人共同审稿,感谢他们对这项工作的同行审稿做出的贡献。
额外的信息
出版商的注意
施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
术语表
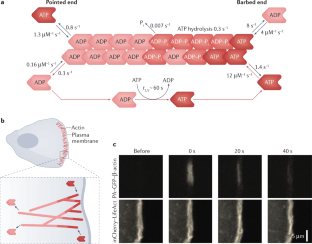
- 带刺的结束
-
肌动蛋白丝快速生长的末端,与尖端相反。在细胞中,肌动蛋白丝的倒钩端通常面向质膜或细胞器。肌动蛋白丝在其带刺的末端聚合产生推力。
- 尖头
-
肌动蛋白丝缓慢生长的末端对于处于稳态的纯肌动蛋白,肌动蛋白丝的分解主要发生在丝的尖端。
- Treadmilling
-
肌动蛋白丝的刺端同时伸长,尖端同时解聚的现象。在稳定状态下,聚合和解聚速率相等,因此长丝具有恒定的长度,单体在长丝中从倒钩端流向尖端。
- Mechanosensing
-
细胞感知其机械环境的能力。来自机械环境的信息往往被转化为生物化学信号,这些信号可以控制细胞的多个过程。
- Fascin
-
一种肌动蛋白捆绑蛋白,将纤维以相似的方向组织成密集的排列。束蛋白1是丝状结构中主要的捆绑蛋白。
- CARMIL
-
参与动物细胞迁移和形态发生的蛋白质家族。CARMILs与运动细胞前缘的capping蛋白(CP)相互作用,控制CP与肌动蛋白丝倒钩末端的结合和CP的分离。
- 应力纤维
-
非肌肉细胞的可收缩的肌动球蛋白束。应力纤维通常通过局灶黏附从其末端与细胞外基质相关联,因此对细胞黏附、形态发生和机械传感很重要。
- 波浪调节复合体
-
(人们)。含有促核因子WAVE的五聚体复合物在被Rac1激活后,WAVE可以结合并激活Arp2/3复合体,形成与细胞突起有关的分支网络。
- 手性过程
-
如果一个物体或过程与其镜像相区别,那么它就是手性的。手性过程可能导致细胞器的不对称分布和细胞水平或组织水平浓度梯度的出现,并可能在生物体水平上出现左右不对称。
- LIM结构域蛋白
-
一个包含一个或多个LIM结构域的蛋白质大家族,其定位于肌动蛋白细胞骨架结构,如应力纤维,在机械应力作用下增强。最著名的蛋白质是zyxin, paxillin和FHL亚家族的成员。
- α连环蛋白
-
参与细胞粘附的复杂调节的蛋白质,主要是作为一种机械敏感的衔接蛋白,将肌动蛋白细胞骨架与称为“钙粘蛋白”的跨膜蛋白连接起来。
- 膨压
-
力,源于细胞内的渗透压,在植物、酵母和细菌中,它将质膜推向细胞壁。
- ENTH/ANTH结构域蛋白
-
参与内吞作用的肌动蛋白和膜结合蛋白家族。这些蛋白质可以将延长的肌动蛋白丝连接到内吞内陷。
权利和权限
根据与作者或其他权利人签订的出版协议,施普林格·自然或其许可方对本文拥有专有权;作者自行存档的接受的手稿版本的这篇文章是完全由这样的出版协议和适用法律的条款管辖。
关于本文
引用本文
Lappalainen, P., Kotila, T., jsamou, A.等。肌动蛋白动力学的生化和机械调节。中华生物医学工程学报,23(2):836-852(2022)。https://doi.org/10.1038/s41580-022-00508-4
录用日期:2022年6月13日
发布日期:2022年8月2日
发行日期:2022年12月
DOI: https://doi.org/10.1038/s41580 - 022 - 00508 - 4
这篇文章是由
-
基于生物材料的机械调节促进无疤痕伤口愈合与功能性皮肤附属物再生
军事医学研究(2024)
-
基于偏振调制的高时空分辨率三维偶极子定向成像
PhotoniX (2024)
-
组织形态和功能调节中的机械状态转变
分子细胞生物学(2024)
-
HKDC1通过将细胞骨架与STAT1激活和PD-L1表达偶联来促进肝癌的肿瘤免疫逃逸
自然通讯(2024)
-
KLF5调控肌动蛋白重塑促进鼻咽癌转移
致癌基因(2024)